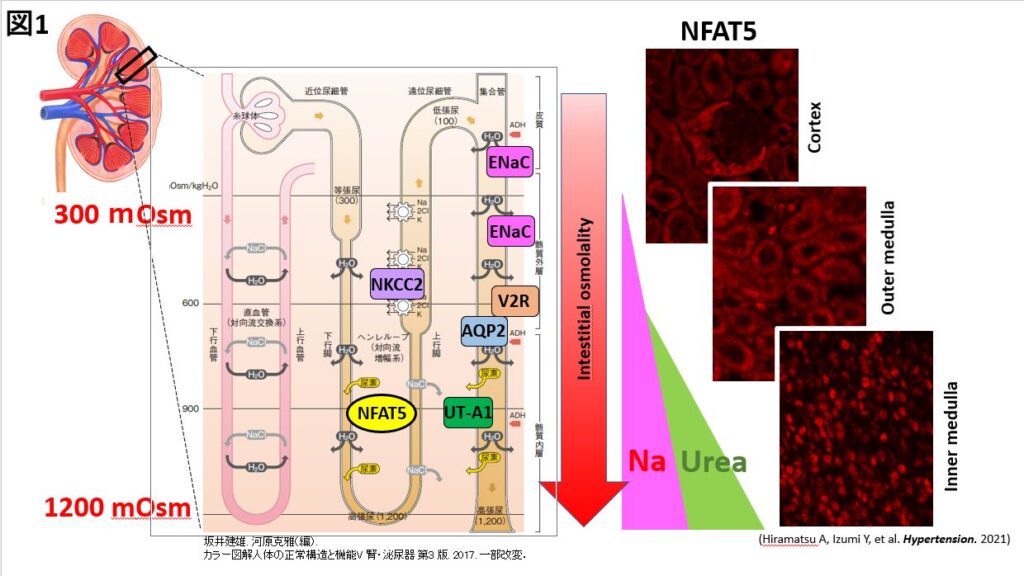
腎臓の重要な役割の一つである、尿の濃縮は、尿細管が皮質ー髄質間でヘアピンカーブを形成する特殊な構造に基づいた、対向流増幅系とよばれる機序によって成り立つ。皮質から髄質にかけて、非常に高度な浸透圧勾配が形成され、この浸透圧勾配によって、集合尿細管の管腔測のAQP2から水が再吸収、すなわち、尿が濃縮が促進されます。間質の浸透圧は、ヘンレの太い上行脚のNKCC2から再吸収されるナトリウムと、髄質集合管のUT-A1から再吸収される尿素の蓄積によって形成されます。ENaCは皮質と、髄質の表層にあたる髄質外層に主に分布しています。
このように、腎臓は、NFAT5により細胞を守りながら浸透圧勾配を形成し、水とNaの再吸収調節に利用しているわけです。
腎臓は、糸球体とそれに続く尿細管を一単位とするネフロンの集合体により形成されており、ネフロンを通して水・電解質の分泌・再吸収を行い、体液の恒常性を維持しています。水の再吸収(尿の濃縮)は、尿細管と腎間質の浸透圧差を利用して行われます(対向流増幅系)。そのため、腎臓は、皮質から髄質にかけて非常に高度な浸透圧勾配を有している点でとてもユニークな臓器です。髄質の間質にはナトリウム(Na)と尿素(urea)が大量に蓄積しており、間質浸透圧は1200mOsm/kg・H2Oにも及ぶため、そこに生存する細胞にとっては非常に苛酷な環境といえます。このような高浸透圧環境で細胞が生存するには、osmoprotective genesと呼ばれる一連の遺伝子群の発現が必須であり、その発現を調節する転写因子としてNFAT5 (nuclear factor of activated T-cells 5)が知られています(図1)。
NFAT5は、免疫反応の制御に重要な役割を果たすNFATファミリーの一員です。しかし、NFAT5はNFAT1~4とは異なり、カルシニューリンにより活性化せず、代わりに高浸透圧環境で活性化します。そのユニークな性質から、NFAT5はTonEBP (tonicity-responsive enhancer-binding protein)またはOREBP (osmotic response element-binding protein)とも呼ばれています。
NFAT5はubiquitousに発現し、活性化すると核内に移動します。間質浸透圧の高い腎臓の髄質ではNFAT5が核内に局在しています。NFAT5は、腎集合管に発現する水チャネルアクアポリン2(AQP2)や尿素トランスポーターUT-A1の発現を転写レベルで調節することがin vitroで示されています。またゲノムワイド関連解析において、NFAT5の多型が高血圧や血清Na高値と関連することが示唆されています。
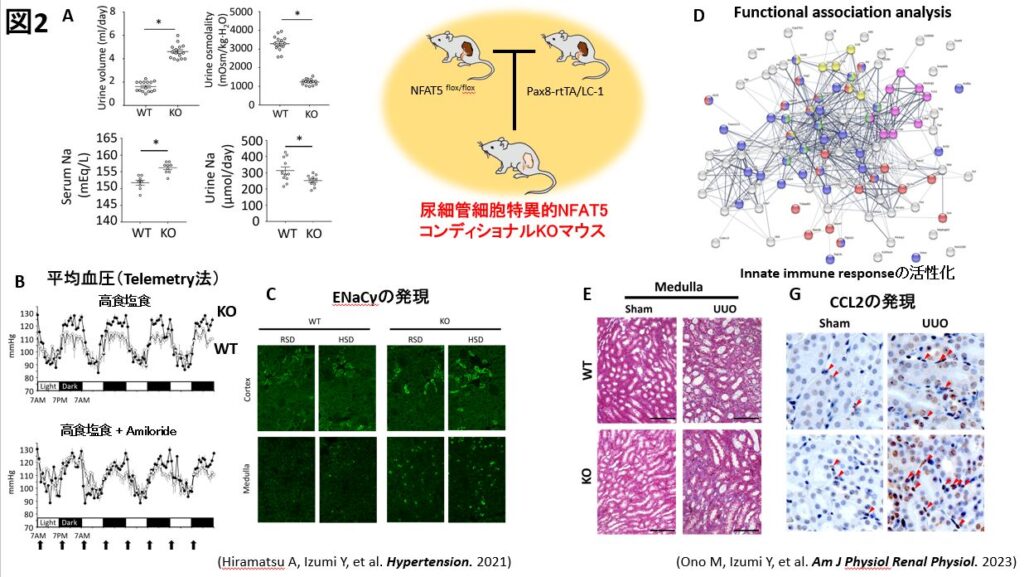
近年、私たちは、腎尿細管細胞特異的薬剤誘導性NFAT5 ノックアウト(KO)マウスを作製し、このマウスがAQP2とUT-A1の発現減少による尿濃縮障害を生じることを明らかにしました(図2A)。また、このマウスは食塩感受性高血圧と血清Na高値を示し(図2B)、その表現型は、上皮型NaチャネルENaCの発現亢進に起因していました(図2C)。そのため、尿濃縮障害を呈しつつも、食餌摂取により塩分と体液が容易に貯留する表現型を有しています(Hiramatsu A, et al. Hypertension. 2021)。
また、KOマウスの腎臓を用いてtranscription start site sequencing (TSS-seq)により遺伝子発現を網羅的に解析したところ、innate immune responseの障害から腎組織のマイルドな炎症を生じていることが示唆されました(図2D)。片側尿管結紮により腎線維化を誘導すると、KOマウスでは、野生型マウスに比し、単球遊走因子であるCCL2 (C-C motif chemokine 2,MCP1)の発現増加とともに線維化が有意に増悪しました(図2F, G)(Ono M, et al. Am J Physiol Renal Physiol. 2023)。
さらに私たちは、NFAT5 KOマウスは加齢とともに腎線維化が自然に発生、進行することも見出しています。これらの結果は、NFAT5もしくは腎臓の浸透圧の制御が高血圧や慢性腎臓病の新たな治療標的となる可能性を示唆しています。本研究を通して、腎臓の体液恒常性維持機構の理解がより深まり、また、食塩感受性高血圧や慢性腎障害に関する新たな知見が得られることを期待しています。
